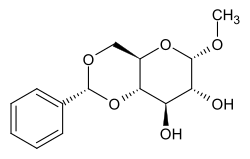
Methyl-4,6-O-benzyliden-α-D-glucopyranosid
| Strukturformel | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| |||||||||||||||||||
| Allgemeines | |||||||||||||||||||
| Name | Methyl-4,6-O-benzyliden-α-D-glucopyranosid | ||||||||||||||||||
| Summenformel | C14H18O6 | ||||||||||||||||||
| Kurzbeschreibung |
beiges Pulver[1] | ||||||||||||||||||
| Externe Identifikatoren/Datenbanken | |||||||||||||||||||
| |||||||||||||||||||
| Eigenschaften | |||||||||||||||||||
| Molare Masse | 282,29 g·mol−1 | ||||||||||||||||||
| Aggregatzustand |
fest | ||||||||||||||||||
| Schmelzpunkt | |||||||||||||||||||
| Sicherheitshinweise | |||||||||||||||||||
| |||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | |||||||||||||||||||
Methyl-4,6-O-benzyliden-α-D-glucopyranosid ist eine chemische Verbindung aus der Gruppe der Monosaccharide. Es ist ein teilgeschütztes Derivat der Glucose, das als Zwischenprodukt in der organischen Synthese verwendet wird. Entscheidende funktionelle Gruppen sind die beiden übrigen freien Hydroxygruppen sowie das Benzyliden-Acetal.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Methyl-4,6-O-benzyliden-α-D-glucopyranosid kann auf verschiedene Weisen synthetisiert werden. Das Edukt ist dabei stets Methyl-α-D-glucopyranosid. Dieses kann zum Beispiel mit Benzaldehyd als Reaktant und Lösungsmittel in Gegenwart von Zinkchlorid bei leicht unter Raumtemperatur zum Produkt umgesetzt werden.[2] Gegebenenfalls ökonomischer ist die Verwendung von 5 Mol-% Vanadyltriflat (VO(TfO)2) als Katalysator bei Austausch des Lösungsmittel zu Acetonitril und Reaktionsführung bei Raumtemperatur.[3]
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Methyl-4,6-O-benzyliden-α-D-glucopyranosid kristallisiert in Form feiner Nadeln.[2][3]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b c Datenblatt Methyl-4,6-O-benzyliden-α-D-glucopyranosid bei Sigma-Aldrich, abgerufen am 21. November 2022 (PDF).
- ↑ a b J. J. Patroni, R. V. Stick: The deoxygenation of some derivatives of methyl 3-amino-3-deoxy-α-D-glucopyranoside. In: Australian Journal of Chemistry. Band 38, Nr. 6, 1985, S. 947–952, doi:10.1071/CH9850947.
- ↑ a b C.-T. Chen, S.-S. Weng, J.-Q. Kao, C.-C. Lin, M.-D. Jan: Stripping off water at ambient temperature: direct atom-efficient acetal formation between aldehydes and diols catalyzed by water-tolerant and recoverable vanadyl triflate. In: Organic Letters. Band 7, Nr. 15, 2005, S. 3343–3346, doi:10.1021/ol051178z.
