Benutzer:MaFecht93/Spielwiese/Chemie/Nazarov-Cyclisierung
| Edukt |
|---|
 Divinylketon R1 = H, Alkyl, Aryl R2 = H, Alkyl, Aryl |
Die Nazarov-Cyclisierung, auch Nazarov-Reaktion genannt, ist eine Namensreaktion der organischen Chemie und wurde in den Vierzigerjahren durch den russischen Chemiker Ivan Nikolaevich Nazarov (* 1906) entdeckt.[1] Bei der Reaktion handelt es sich um eine Synthesereaktion für Cyclopentenone aus Divinylketonen und deren Präkursoren.[2][3]
Unter dem Begriff der Nazarov-Cyclisierung werden weitere Reaktionen mit anderen Substraten aber ähnlichem Reaktionsmechanismus zusammengefasst.
Übersichtsreaktion
[Bearbeiten | Quelltext bearbeiten]Bei der von Nazarov ursprünglich beschriebenen Cyclisierung werden stöchiometrische Mengen einer Lewis-Säure zur Aktivierung des Divinylketons verwendet.[1][2][3] Die folgende Übersicht zeigt eine Variante mit Wasserstoff als Substituent (R1 = H und R2 = H):
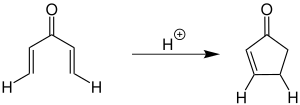
Neben Wasserstoff können eine Vielzahl weiterer Organylgruppen verwendet werden. Sowohl für R1 als auch R2 sind Alkyl- und Arylgruppen möglich.[3][4]
Werden bei der Nazarov-Cyclisierung unsymmetrische Divinylketone eingesetzt, so läuft die Reaktion nach folgendem Reaktionsschema ab:

Als Produkt entsteht ein Gemisch der Verbindungen 1 und 2.
Mechanismus
[Bearbeiten | Quelltext bearbeiten]Der Mechanismus der Nazarov-Cyclisierung ist sehr gut erforscht. Es handelt sich dabei im Wesentlichen um einen elektrocyclischen Mechanismus mit konrotatorischem Ringschluss.[5][6]

Im ersten Reaktionsschritt wird das Divinylketon 1 unter dem Einfluss einer Säure zum Hydroxypentadienylkation 2 protoniert. Anschließend reagiert Substanz 2 mittels Ringschluss zum Cyclopentenylkation 3. Durch anschließende Deprotonierung des Kations 3 bildet sich zuerst das Enol 4, welches durch Keto-Enol-Tautomerie dann zum α,β-ungesättigten Keton 5 reagiert.
Die Entstehung eines Produktgemisches bei der Umsetzung von unsymmetrischen Divinylketonen ist auf folgende mesomere Grenzformeln des im Mechanismus auftretenden Cyclopentenylkations zurückzuführen:[5]

Beide mesomeren Grenzformeln können, wie im Mechanismus gezeigt, deprotoniert werden. Folglich entstehen zwei Reaktionsprodukte.
Anwendung
[Bearbeiten | Quelltext bearbeiten]Die bei der Reaktion entstehenden Produktgemische stellen einen großen Nachteil bei dem Einsatz in der chemischen Industrie dar. Dieser wird durch den Einsatz folgender Trimethylsilyl-substituierten Carbonylverbindungen verhindert:[5]

Dieses Verfahren wurde erstmals von dem Chemiker Scott Denmark publiziert.[5] Da sich Divinylketone mit verschiedensten Substituenten relativ leicht synthetisieren lassen, findet die Nazarov-Cyclisierung diverse Anwendungsmöglichkeiten. Vor allem die Verwendung silylierter Carbonylverbindungen spielt eine wichtige Rolle bei der Synthese cyclopentanoider Systeme, welche ihre Anwendung in der Naturstoffchemie finden.[5][6]
Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ a b Nazarov, I.N., Zaratskaya, I. I. Derivates of acetylene. XXVII. Hydration of divinylacetylene. Bull. acad. sci. U.R.S.S., Classe sci. chim. 1942, 200–209.
- ↑ a b Nazarov, I. N., Zaretskaya, I.I. Structure of products of hydration of divinylethynyl hydrocarbons. Zh. Obshch. Khim. 1957, 27, 693–713.
- ↑ a b c Nazarov, I. N., Zaretskaya, I. I., Sorkina, T. I. Cyclopentanolones from the cyclization of divinyl ketones. Zh. Obshch. Khim. 1960, 30, 746–754
- ↑ Zerong Wang: Comprehensive Organic Name Reactions and Reagents. John Wiley & Sons, New Jersey '''2009''', ISBN 978-0-471-70450-8, S. 2011–2015.
- ↑ a b c d e Thomas Laue und Andreas Plagens: Namen- und Schlagwort-Reaktionen der Organischen Chemie, Teuber Verlag, Wiesbaden, 2006, Seiten 240–242, ISBN 3-8351-0091-2.
- ↑ a b László Kürti und Barbara Czakó.: Strategic Applications of Named Reactions in Organic Synthesis: Background and Detailed Mechanisms, Elsevier Academic Press, 2005, S. 304–305, ISBN 978-0-12-429785-2.
