Calciumchlorid
| Kristallstruktur | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
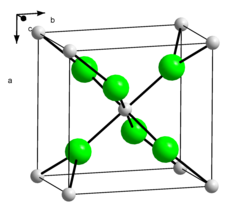
| ||||||||||||||||||||||
| _ Ca2+ _ Cl− | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | Calciumchlorid | |||||||||||||||||||||
| Andere Namen | ||||||||||||||||||||||
| Verhältnisformel | CaCl2 | |||||||||||||||||||||
| Kurzbeschreibung |
farb- und geruchlose, hygroskopische Kristalle [3] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Arzneistoffangaben | ||||||||||||||||||||||
| ATC-Code | ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse |
| |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte | ||||||||||||||||||||||
| Schmelzpunkt | ||||||||||||||||||||||
| Siedepunkt |
1670 °C[3] | |||||||||||||||||||||
| Löslichkeit |
gut in Wasser (740 g·l−1 bei 20 °C)[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
Calciumchlorid (auch Kalziumchlorid) ist ein Chlorid des Erdalkalimetalls Calcium mit der Verhältnisformel CaCl2. Calcium liegt dabei in der Oxidationsstufe +2 vor, Chlor hat die Oxidationsstufe −1.
Geschichte
[Bearbeiten | Quelltext bearbeiten]Um 1860 gelang den Chemikern Robert Wilhelm Bunsen und Augustus Matthiessen die erste Reindarstellung des Elementes Calcium durch Schmelzelektrolyse von Calciumchlorid.
Vorkommen
[Bearbeiten | Quelltext bearbeiten]Calciumchlorid kommt in der Natur gelöst in Salzsolen vor.
Wasserhaltiges Calciumchlorid bildet die seltenen Minerale Sinjarit (Dihydrat) und Antarcticit (Hexahydrat). Das Anhydrid kommt als Hydrophilit vor.
Gewinnung und Darstellung
[Bearbeiten | Quelltext bearbeiten]Calciumchlorid wird aus Salzsäure und Calciumcarbonat hergestellt:
Technisch wird Calciumchlorid als Abfallprodukt bei der Sodaherstellung nach dem Solvay-Verfahren – und zwar bei der Rückgewinnung des Ammoniaks aus dem dabei entstandenen Ammoniumchlorid – erhalten:
Eigenschaften
[Bearbeiten | Quelltext bearbeiten]Calciumchlorid ist ein Salz. Calcium und Chlor liegen aufgrund des großen Elektronegativitätsunterschiedes ionisch vor. Die Bindung erfolgt somit über elektrostatische Wechselwirkungen. Calciumchlorid bildet farblose Kristalle, die eine verzerrte Rutil-Struktur ausbilden (orthorhombisch, Raumgruppe Pnnm (Raumgruppen-Nr. 58)).[8]
Calciumchlorid bildet in Reinform farblose Kristalle und ist in wasserfreiem Zustand stark hygroskopisch. Es nimmt leicht Wasser aus der Umgebung auf und bildet dabei einen Hydrat-Komplex. Es sind mehrere kristalline Hydrate bekannt. Das Dihydrat kristallisiert orthorhombisch in der Raumgruppe Pbcn (Raumgruppen-Nr. 60) mit den Gitterparametern a = 5,893 Å, b = 7,469 Å und c = 12,07 Å.[9] Das Tetrahydrat ist polymorph. Die α-Form kristallisiert triklin, Raumgruppe P1 (Nr. 2), mit den Gitterparametern a = 6,593 Å, b = 6,367 Å, c = 8,561 Å, α = 97,83°, β = 93,5° und γ = 110,6°.[10] Die β-Form hat eine monokline Struktur mit der Raumgruppe P21/c (Nr. 14), Gitterparameter a =8,923 Å, b = 10,22 Å, c = 12,79 Å und β = 114,7°.[11] Die γ-Form des Tetrahydrats kristallisiert ebenfalls monoklin in der Raumgruppe P21/c (Nr. 14) mit den Gitterparametern a = 6,139 Å, b = 7,667 Å, c = 8,901 Å und β = 111,0°.[12] Das Hexahydrat hat eine trigonale Struktur, Raumgruppe P321 (Nr. 150) mit den Gitterparametern a = 7,876 Å und c = 8,561.[13] Es sind auch entsprechende Komplexe mit Ammoniak bekannt (CaCl2·n (NH3) mit n=1,2,4,8).[14]
Das wasserfreie Calciumchlorid löst sich in Wasser exotherm.
Die Verbindung bildet mit Methanol und Ethanol bei Raumtemperatur stabile Solvate. Mit Methanol wurden Solvate der Stöchiometrie 1:2, 1:3, 1:4, 1:6 und 1:8 bezogen auf Calciumchlorid und mit Ethanol Solvate der Stöchiometrie 1:2, 1:3, 1:4 und 1:6 bezogen auf Calciumchlorid hergestellt und charakterisiert.[15]
Reaktionen
[Bearbeiten | Quelltext bearbeiten]Wasserfreies Calciumchlorid reagiert mit Wasser unter Bildung eines Hexahydrat-Komplexes und starker Wärmeentwicklung (exotherme Reaktion mit ΔH < 0):
Das Auflösen des Hexahydrat-Komplexes in Wasser führt im Gegensatz zu wasserfreiem Calciumchlorid zu einer starken Abkühlung (endotherme Reaktion). Beide Calciumchlorid-Formen sind zudem gut löslich in Ethanol. Das im Hexahydrat gebunde Kristallwasser ist nur locker gebunden und entweicht schon beim Erhitzen auf 30 °C, das Calciumchlorid löst sich dann im eigenen Kristallwasser. Grundsätzlich lässt sich Calciumchlorid bei etwa 220 °C zum Großteil entwässern, dazu reicht ein Backofen. Allerdings ist dabei Vorsicht geboten, da das wässrige Calciumchlorid bei zu schnellem Aufheizen u. a. Salzsäuredämpfe (Chlorwasserstoff) entwickelt.[16] Um komplett wasserfreies Calciumchlorid zu erhalten, muss die Lösung bis zur Schmelztemperatur 772 °C erwärmt werden.

Verwendung
[Bearbeiten | Quelltext bearbeiten]Im Labor
[Bearbeiten | Quelltext bearbeiten]Wasserfreies Calciumchlorid ist aufgrund seiner Hygroskopie ein wichtiges Trocknungsmittel im Labor, beispielsweise im Exsikkator, und in der technischen Chemie für Gase und Flüssigkeiten.
Darüber hinaus wird es als Streusalz (Auftaumittel) sowie als Hexahydrat zur Herstellung von Kältemischungen verwendet.
Im Bauwesen
[Bearbeiten | Quelltext bearbeiten]
Anwendungsfelder im Bauwesen sind die Trocknung von Wohnräumen, der Einsatz als Frostschutzmittel, als Abbindebeschleuniger im Beton sowie als Staubbindemittel (zum Beispiel auf Baustellen und als Besatz bei Sprengarbeiten). Die Verwendung von Calciumchlorid als Abbindebeschleuniger in Beton wurde in Deutschland wegen der korrosiven Wirkung des Chlorids auf die Eisenarmierung 1963 verboten.[17]
Dem Füllwasser von betonierten Schwimmbecken wird Calciumchlorid zugesetzt, um die Wasserhärte zu erhöhen und nach dem Prinzip vom kleinsten Zwang die Betonerosion durch Lösung von Calciumverbindungen aus dem Beton zu reduzieren.
Außer als Frostschutzmittel wird die größte Menge Calciumchlorid zum Binden von Sand und Staub auf unbefestigten Straßen eingesetzt. Da es stark hygroskopisch ist, zieht eine auf der Straße aufgebrachte konzentrierte Calciumchloridlösung Feuchtigkeit an und unterdrückt den Abtrag des Straßenstaubs. Die Straßenoberfläche muss seltener eingeebnet und die Oberfläche seltener erneuert werden.[18]
In der Medizin
[Bearbeiten | Quelltext bearbeiten]Medizinisch wird Calciumchlorid bei Calciummangelzuständen, insbesondere im Rahmen der Bluttransfusion citrathaltiger Erythrozyten-Konzentrate, eingesetzt oder dient als Notfallmedikament zur Behandlung einer schweren Hyperkaliämie.[19]
In der Lebensmittelindustrie
[Bearbeiten | Quelltext bearbeiten]Die Lebensmittelindustrie verwendet es als Komplexbildner, Geschmacksverstärker und Stabilisator (unter anderem bei der Trinkwasseraufbereitung). Es ist in der EU als Lebensmittelzusatzstoff E 509 zugelassen. Die tägliche Aufnahmemenge wird mit 160–345 mg angenommen.[20]
Als Festigungsmittel wird es Dosengemüse und aufgeschnittenen Früchten zugesetzt. Ebenfalls dient es zur Gerinnung von Eiweißen in der Lebensmittelherstellung, zum Beispiel bei der Produktion von Käse, Tofu oder künstlichem Kaviar.[21] Bei der Käseherstellung wird Calciumchlorid manchmal der Milch zugesetzt, um die Eigenschaften des ausgefällten Kaseins zu verbessern.
In Sportgetränken dient es als Calcium-Lieferant (Elektrolyt).
Aufgrund des salzigen Geschmacks kann es Speisesalz in Salzgurken und Sauergemüse ersetzen.
Beim Bierbrauen wird Calciumchlorid verwendet, um den Mineraliengehalt des Brauwassers anzugleichen und Geschmack und Hefewachstum zu beeinflussen.
Calciumchlorid wird zur Oberflächenbehandlung von Obst eingesetzt. Äpfel werden in der späten Wachstumsphase behandelt, um die Mangelkrankheit Stippe und andere Beeinträchtigungen zu vermeiden.[22]
Unter Ausnutzung der exothermen Hydratation bei der Reaktion mit Wasser findet Calciumchlorid Einsatz zur Erwärmung von Fertiggetränken.
In der Molekularbiologie dient es zur Herstellung kompetenter Zellen. Calciumionen verändern hierbei die Permeabilität der Zellmembran und steigern so das Aufnahmepotenzial der Zelle für DNS.
Sonstiges
[Bearbeiten | Quelltext bearbeiten]In der Meerwasseraquaristik wird Calciumchlorid genutzt, um den Calciumgehalt zu erhöhen.
Weblinks
[Bearbeiten | Quelltext bearbeiten]Einzelnachweise
[Bearbeiten | Quelltext bearbeiten]- ↑ Eintrag zu E 509: Calcium chloride in der Europäischen Datenbank für Lebensmittelzusatzstoffe, abgerufen am 27. Juni 2020.
- ↑ Eintrag zu CALCIUM CHLORIDE in der CosIng-Datenbank der EU-Kommission, abgerufen am 24. Februar 2020.
- ↑ a b c d e f g h Eintrag zu Calciumchlorid in der GESTIS-Stoffdatenbank des IFA, abgerufen am 18. Februar 2017. (JavaScript erforderlich)
- ↑ a b c d e Richard C. Ropp: Encyclopedia of the Alkaline Earth Compounds. Newnes, 2012, ISBN 0-444-59553-8, S. 54 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Datenblatt Calcium chloride dihydrate, for molecular biology, ≥99% bei Sigma-Aldrich, abgerufen am 1. Mai 2017 (PDF).
- ↑ Eintrag zu Calcium chloride im Classification and Labelling Inventory der Europäischen Chemikalienagentur (ECHA), abgerufen am 1. Februar 2016. Hersteller bzw. Inverkehrbringer können die harmonisierte Einstufung und Kennzeichnung erweitern.
- ↑ Eintrag zu Calcium chloride anhydrous in der ChemIDplus-Datenbank der United States National Library of Medicine (NLM) (Seite nicht mehr abrufbar)
- ↑ A.K. van Bever, W. Nieuwenkamp: Die Kristallstruktur von Calciumchlorid, CaCl2. In: Zeitschrift für Kristallographie, Kristallgeometrie, Kristallphysik, Kristallchemie, 1935, 90, S. 374–376.
- ↑ A. Leclaire, M.M. Borel: Le dichlorure de calcium dihydrate. In: Acta Crystallographica, B33, 1977, S. 1608–1610, doi:10.1107/S0567740877006645.
- ↑ A. Leclaire, M.M. Borel: Liaisons hydrogene et coordination du calcium dans les cristaux de CaCl2·4 H2O α. In: Acta Crystallographica, B35, 1979, S. 585–588, doi:10.1107/S0567740879004209.
- ↑ A. Leclaire, M.M. Borel: La forme β du dichlorure de calcium tetrahydrate. In: Acta Crystallographica, B34, 1978, S. 900–902, doi:10.1107/S0567740878004288.
- ↑ A. Lecklaire, M.M. Borel, J.C. Monier: La forme γ du dichlorure de calcium tétrahydraté. In: Acta Crystallographica, B36, 1980, S. 2757–2759, doi:10.1107/S0567740880009909.
- ↑ P.A. Agron, W.R. Busing: Calcium and strontium dichloride hexahydrates by neutron diffraction. In: Acta Crystallographica, C42, 1986, S. 141–143, doi:10.1107/S0108270186097007.
- ↑ S. Westman, P.-E. Werner, T. Schuler, W. Raldow: X-Ray Investigations of Ammines of Alkaline Earth Metal Halides. I. The Structures of CaCl2(NH3)8, CaCl2(NH3)2 and the Decomposition Product CaClOH. In: Acta Chemica Scandinavica, 35A, 1981, S. 467–472, doi:10.3891/acta.chem.scand.35a-0467.
- ↑ Korhammer, K.; Mihaly, J.; Balint, S.; Trif, L.; Vass, A.; Tompos, A.; Talas, E.: Reversible formation of alcohol solvates and their potential use for heat storage in J. Therm. Anal. Calorim. 138 (2019) 11–33, doi:10.1007/s10973-019-08090-2.
- ↑ Hans Lohninger: Calciumchlorid als Luftentfeuchter. In: anorganik.chemie.vias.org. 8. August 2013, abgerufen am 26. März 2023.
- ↑ Jochen Stark: Dauerhaftigkeit von Beton. Springer-Verlag, 2013, ISBN 978-3-642-35278-2, S. 263 (eingeschränkte Vorschau in der Google-Buchsuche).
- ↑ Dust: Don't Eat It! Control It! In: Road Management & Engineering Journal. US Roads (TranSafety Inc.), 1. Juni 1998, archiviert vom am 29. Oktober 2007; abgerufen am 9. August 2006.
- ↑ European-Resuscitation-Council-Guidelines-2021: Cardiac Arrest in special circumstances.
- ↑ Calcium Chloride SIDS Initial Assessment Profile, UNEP Publications, SIAM 15, Boston, 22–25 October 2002, pp. 13–14.
- ↑ Apple Caviar Technique. In: StarChefs Studio. StarChefs.com, April 2004, abgerufen am 9. August 2006.
- ↑ "Cork Spot and Bitter Pit of Apples", Richard C. Funt and Michael A. Ellis, Ohioline.osu.edu/factsheet/plpath-fru-01




